Introduction
Le Gamma-ButyroLactone (GBL), est un précurseur du Gamma-HydroxyButyrone (GHB). Le GBL est synthétisé par le foie en GHB avec des effets quasi-identiques. Il agit sur le système gabaergique comme l’alcool et les benzodiazépines.
Le GBL se présente sous forme d’un liquide incolore, dilué cinquante à cent fois dans une boisson (eau, jus) lorsqu’il est consommé. L’usage du GBL/GHB demeure assez spécifiquement lié au milieu festif homosexuel. La population usagère est majoritairement masculine, bien insérée et appartenant à des catégories socioprofessionnelles plutôt élevées selon les données issues du dispositif Tendances Récentes et Nouvelles Drogues (TREND) de l’Observatoire Français des Drogues et de la Toxicomanie (OFDT) [1].
Cas clinique
Mr X est un patient de 30 ans, homosexuel, qui a consulté pour la première fois en octobre 2014 au Centre de Soins d’Accompagnement et de Prévention en Addictologie (CSAPA) pour une addiction au GBL. Il avait substitué il y a 3 ans une importante consommation récréative d’alcool par des prises de GBL de plus en plus fréquentes et importantes.
Il usait lors du premier contact avec le CSAPA d’environ 50 cl de GBL par mois, acheté sur internet. Les prises étaient pluriquotidiennes, à raison de 2 à 4 millilitres toutes les 2 heures, y compris la nuit et non diluées dans une boisson. Une forte dépendance physique était déjà installée et il existait des signes de sevrage chaque matin au réveil, caractérisés par des tremblements, des sueurs, une forte angoisse et un craving important pour le GBL. Les conséquences de cette addiction étaient notamment la contamination accidentelle par le Virus de l’Immunodéficience Humaine (VIH) lors de relations sexuelles à risque sous l’influence du produit et une difficulté croissante à maintenir son emploi de banquier.
Mr X avait également une co-consommation de cannabis à raison de 3 joints par jour et une consommation festive très occasionnelle de cocaïne et de MDMA. Il buvait encore de l’alcool occasionnellement.
A son admission au CSAPA, Mr X a formulé une demande de sevrage ambulatoire du GBL. Nous l’avons donc accompagné dans son projet à l’aide de consultations médicales régulières et d’un traitement médicamenteux par clorazépate jusqu’à 120 mg par jour. Devant l’impossibilité constatée par le patient de diminuer seul ses consommations, nous avons ensuite rapidement opté pour un sevrage hospitalier programmé début février 2015 en unité d’addictologie de niveau 2.
Dès lors que l’hospitalisation a été organisée, Mr X s’est montré plus anxieux à l’idée du sevrage et a majoré ses consommations de GBL auxquelles il a adjoint pendant quelques jours des prises d’alcool quotidiennes et une surconsommation de clorazépate.
Il a finalement présenté une attaque panique le 27 décembre durant laquelle il a d’abord pris une forte dose de GBL et de clorazépate avant de se débarrasser brutalement dans son évier de l’ensemble de ces produits.
Il s’est finalement présenté aux urgences où il a été hospitalisé le jour même vers 19 heures. Il présentait un tableau de crise d’angoisse aiguë avec des idéations suicidaires et hétéro-agressives non scénarisées ainsi qu’une agitation psychomotrice. La biologie initiale a retrouvé un taux toxique de nordazepam et une alcoolémie négative. Le reste du bilan était sans particularité hormis une élévation isolée des ASpartate AminoTransférases (ASAT). Le GBL n’a pas été dosé mais le patient rapporte sa dernière prise de 4 ml moins de 2 heures avant son arrivée aux urgences.
Après un examen somatique normal réalisé par le médecin urgentiste, Mr X a été pris en charge par le psychiatre de garde vers 22h. Il a rapidement reçu 20 mg d’olanzapine per os afin d’apaiser son agitation. A 5h30 le 28 décembre, le médecin urgentiste a noté l’apparition d’un syndrome confusionnel avec une majoration de l’agitation psychomotrice qui a nécessité une contention physique et une prescription de cyamémazine 100 mg per os. A 23h ce même jour, le tableau clinique s’aggrave encore avec l’apparition d’hallucinations visuelles, de sueurs et de tremblements. Le score de Cushman est noté à 14 et le traitement par olanzapine est renouvelé à 10 mg avec adjonction de lorazepam à 2,5 mg toutes les 2 heures.
Mr X est transféré dans la nuit en unité de soins continus pour un tableau de sevrage avec delirium. Un protocole thérapeutique est immédiatement mis en place, comprenant : une hyperhydratation, une vitaminothérapie B1 et B6 et une prescription de diazepam en intraveineux à la posologie de 10 mg par heure. L’olanzapine n’a pas été poursuivie mais de l’haloperidol à 2 mg par jour a été ajouté deux jours plus tard devant la persistance de crises d’agitation. Mr X a pu être transféré en service psychiatrique conventionnel après un séjour de 6 jours en soins continus et son traitement de sortie comprenait alors de l’halopéridol à 2 mg par jour, du diazépam à 8 mg par jour et du zolpidem à 10 mg au coucher.
Il est actuellement toujours en soins sur le CSAPA et abstinent de GBL depuis son sevrage. Il souffre aujourd’hui d’un épisode dépressif majeur d’intensité sévère qui régresse progressivement avec la mise en place d’un suivi en hôpital de jour 4 demi-journées par semaine et d’un traitement antidépresseur par venlafaxine à la posologie de 300 mg par jour. Il a présenté 2 très brèves rechutes avec la GBL depuis son sevrage.
Discussion
1. Importance du phénomène
D’après l’Agence Nationale de Sécurité du Médicament (ANSM), 177 cas d’intoxication au GBL dont 97 expositions accidentelles, 80 intoxications volontaires incluant 63 cas de consommation dans un contexte d’abus ou de dépendance, 7 cas de suspicion de soumission chimique et 10 tentatives de suicide ont été identifiés en France entre 2005 et 2009 par le réseau de toxicovigilance (CAPTV) et le réseau d’addictovigilance (CEIP). Le bilan des cas notifiés entre octobre 2009 et avril 2011 fait état de 34 nouveaux cas, parmi lesquels 28 cas d’intoxications aiguës dont un décès. Les cas d’intoxications volontaires concernent majoritairement de jeunes hommes qui consomment du GBL dans un contexte festif [2].
L’Observatoire Français des Drogues et Toxicomanies (OFDT) signale que le GBL, facile d’accès sur internet, a progressivement remplacé l’usage du GHB. Dans les milieux du clubbing homosexuel à Paris, il semble que dès 2007, seul le GBL circule [3, 4]. Une étude in situ de 2009 auprès de la population fréquentant les clubs parisiens retrouve une prévalence de 22,4% de consommateurs de GBL dans la population étudiée. Les consommateurs sont majoritairement de jeunes hommes de moins de 25 ans [5].
Une étude suisse a analysé 141 cas d’exposition au GHB et au GBL rassemblés entre 1995 et 2003 par le centre antipoison Suisse de Zurich [6]. Sur les 141 dossiers, 7 concernaient un syndrome de sevrage [7, 8] chez des usagers chroniques. Ces 7 patients présentaient un tableau clinique comprenant une tachycardie, une poussée hypertensive, des tremblements, de l’agitation, une anxiété, des hallucinations et une insomnie qui ont parfois persisté plusieurs jours [9-12]. D’autre part plusieurs articles rapportent des cas similaires de syndrome de sevrage grave au GHB et au GBL [13-16], rappelant que la prise chronique à des doses élevées de ces produits induit une dépendance psychique et physique forte. [8, 17]
2. Législation française sur le GBL
En France, le GHB est inscrit sur la liste des stupéfiants depuis 1999. Concernant le GBL, suite à l’augmentation significative de sa consommation à des fins récréatives et des comas suivi de réanimation chez plusieurs usagers, la vente et la cession au public de GBL a été interdite, par arrêté du 2 septembre 2011 [18]. « Le Ministère chargé de la Santé a décidé d’interdire (…) la vente et la cession au public du Gamma-Butyrolactone (GBL) et du 1,4 butanediol (1,4-BD), deux produits qui entrent notamment dans la synthèse du gamma-hydroxybutyrate, plus connu dans le grand public sous le nom de GHB ou de « drogue du viol », classé comme stupéfiant depuis 1999. » Cette interdiction touche aussi les produits manufacturés contenant une concentration, de GBL ou de 1,4-BD, supérieure à 10% et/ou d’un volume de plus de 100 ml. Les sanctions pénales prévues en cas de vente ou de cession au public du GBL et du 1,4-BD sont de 3 ans d’emprisonnement et de 45 000 euros d’amende.
Contrairement au GHB, le GBL est simplement inscrit sur la liste des produits surveillés et les industriels sont tenus de déclarer tout soupçon d’utilisation détournée. D’après la Mission Interministérielle de Lutte contre les Drogues Et les Conduites Addictives (MILDECA), il n’est pas envisageable d’inscrire le GBL sur la liste des stupéfiants ou sur celle des précurseurs chimiques contrôlés, du fait de son utilisation en très grandes quantités dans l’industrie.
Il apparaît donc nécessaire de réfléchir à une communication ciblée vers les populations concernées à propos des risques encourus lors de la consommation de GBL ou de 1,4-BD. Ceci dans une optique de réduction des risques liés à l’ingestion de ces substances (soumission chimique, surdosage et dépendance) et notamment lors de mélanges avec de l’alcool ou d’autres drogues [19].
3. Intérêt du baclofène dans la prise en charge d’une addiction à la GBL ?
La prise en charge du sevrage de GHB/GBL est déjà largement décrite dans la littérature et comprend systématiquement de fortes posologies de benzodiazépines, notamment du diazépam, comme dans notre cas clinique [20]. La difficulté du sevrage semble surtout résider dans les posologies très élevées de benzodiazépines nécessaires pour prévenir les complications du sevrage et notamment le delirium.
Cette stratégie thérapeutique s’avère parfois même insuffisante et nécessite l’utilisation d’autres molécules comme le phénobarbital ou le baclofène.
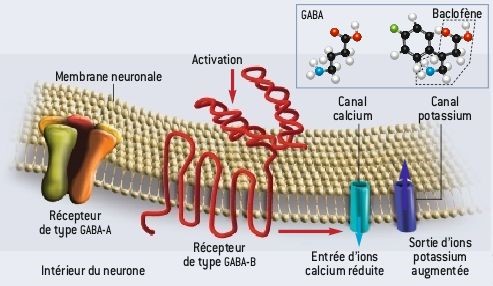
En effet, l’action du GHB au niveau du système nerveux central est principalement médiée par le récepteur GABA-B [21, 22]. Or les benzodiazépines sont des agonistes du récepteur GABA-A ce qui peut expliquer pourquoi leur utilisation dans le sevrage en GHB est parfois insatisfaisante et nécessite un monitorage long [23]. Dans ce contexte, un agoniste du récepteur GABA-B, comme le baclofène, pourrait être un traitement plus spécifique et efficace du syndrome de sevrage.
Un case report de 2008 [24] rapporte l’efficacité du baclofène prescrit à 5 puis 10 mg 3 fois par jour, chez une femme de 61 ans admise pour sevrage de GHB. D’autre part, un essai clinique est en cours de réalisation par Kamal et al. sur l’intérêt du baclofène comme traitement substitutif ou de maintenance de l’abstinence chez des patients présentant une addiction au GHB ou à ses précurseurs [25]. Les résultats ne sont pas encore publiés mais on retrouve déjà dans la littérature un case report de la même équipe d’une patiente de 21 ans ayant fait un coma lors d’une consommation de GHB alors qu’elle était en cours de traitement par baclofène 40 mg par jour depuis 2 mois dans le cadre d’un essai clinique sur son utilisation comme traitement de maintien de l’abstinence dans l’addiction au GHB [26]. L’intoxication a été caractérisée par un coma d’installation rapide associé à une détresse respiratoire.
Au total, le baclofène semble avoir un intérêt en aigu et à de faibles posologies (30-40 mg par jour) dans la prise en charge d’un syndrome de sevrage au GHB afin d’en réduire la durée et les complications. Par contre, un traitement de maintenance au baclofène en prévention de la rechute présente un risque de coma grave en cas de consommation associée de GHB. D’autre part il convient d’être particulièrement attentif lors de la prescription de baclofène dans d’autres indications à la prise concomitante, même occasionnelle, de GHB ou de ses précurseurs en raison comme nous l’avons vu du risque de coma par cumulation des effets des 2 substances [26].
Conclusion
Nous rapportons ici, le cas d’un syndrome de sevrage grave chez un patient dépendant au GBL, ayant nécessité une prise en charge de plusieurs jours en unité de soins continus, malgré l’administration de fortes posologies de benzodiazépines.
La littérature suggère que dans ce cas, l’utilisation de faibles posologies de baclofène, un agoniste GABA-B, entre 30 et 40 mg par jour, pourrait réduire la durée et les complications du sevrage.
Nous avons découvert l’utilisation possible du baclofène dans cette indication qu’après avoir eu à traiter ce cas, en faisant des recherches dans la littérature.
Bibliographie
- [1] Bello P-Y, Toufik A, Gandilhon M, Giraudon I, Phénomènes émergents liés aux drogues en 2003 – Cinquième rapport national du dispositif TREND, OFDT, 2004
- [2] Direction générale de la Santé Paris, Communiqué de presse, Interdiction de l’offre et de la cession au public de la GBL et du 1,4-BD, 8 septembre 2011
- [3] Beck, F., S. Legleye, et al., Les drogues à 17 ans, évolution, contextes d’usage et prises de risque. Tendances, 2006 49: 6
- [4] Wood DM, Nicolaou M, Dargan PI, Epidemiology of recreational drug toxicity in a nightclub environment, Subst Use Misuse, 2009, 44, 11, 1495-502
- [5] Benchaar M, Le GBL : détournement d’un solvant industriel à visée psychodysleptique. Une enquête in situ, Thèse pour le doctorat en Médecine, Université Paris 7 Diderot, 2010
- [6] Liechti M, Kupferschmidt H. g-hydroxybutyrate (GHB) and g-butyrolactone (GBL): analysis of overdose cases reported to the Swiss Toxicological Information Centre. Swiss Med Wkly. 2004; 134: 534-537
- [7] Schneir AB, Ly BT, Clark RF. A case of withdrawal from the GHB precursors gamma-butyrolactone and 1,4-butanediol. J Emerg Med. 2001; 21 (1):31-33
- [8] Dyer JE, Roth B, Hyma BA. Gamma-hydroxybutyrate withdrawal syndrome. Ann Emerg Med. 2001; 37: 147-53
- [9] Donovan JW. Gamma-hydroxybutyrate, gamma-butyrolactone, and butanediol – abuse and effects. J Toxicol Clin Toxicol 2000; 38(2): 183
- [10] Zvosec DL, Smith SW, Ladmer D. Gamma Hydroxybutyrate Withdrawal Syndrome in the Emergency Department : Clinical Cours and Autonomic Instability. Ann Emerg Med 2006; 48(4): 335
- [11] Dyer JE, Roth B, Hyma BA. GHB withdrawal syndrome: eight cases. J Toxicol Clin Toxicol 1999; 37(5): 650
- [12] Chin MY, Kreutzer RA. Acute Poisoning from gamma-Hydroxybutyrate in California. West J Med 1992; 156 : 380-384
- [13] Indrani S. Bhattacharya Fiona Watson Malcolm Bruce A Case of Gamma-Butyrolactone Associated with Severe Withdrawal Delirium and Acute Renal Failure Eur Addict Res 2011;17:169–171
- [14] Ghio L, Cervetti A, Respino M, Belvederi Murri M, Amore M, Management and Treatment of Gamma Butyrolactone Withdrawal Syndrome: A Case Report and Review Journal of Psychiatric Practice Vol. 20, No. 4 July 2014
- [15] Wood DM, Brailsford AD, Dargana PI, Acute toxicity and withdrawal syndromes related to gamma-hydroxybutyrate (GHB) and its analogues gamma-butyrolactone (GBL) and 1,4-butanediol (1,4-BD)1, Drug Test. Analysis 2011, 3, 417–425
- [16] Zepf FD et al. A 16-Year-Old Boy with Severe gamma-Butyrolactone (GBL) withdrawal delirium, Pharmacopsychiatry 2009; 42: 202–203
- [17] Galloway GP, Frederick SL, Staggers F, Jr et al. Gamma-hydroxybutyrate: an emerging drug abuse that causes physical dependence. Addiction 1997; 92: 89-96.
- [18] JORF n°0208 du 8 septembre 2011, Arrêté du 2 septembre 2011 portant application d’une partie de la réglementation des stupéfiants à la gamma-butyrolactone (GBL), au 1,4-butanediol (1,4 BD) et aux produits qui en contiennent
- [19] Wood DM, Warren-Gash C, Ashraf T et al., Medical and legal confusion surrounding gamma-hydroxybutyrate (GHB) and its precursors gamma-butyrolactone (GBL) and 1,4-butanediol (1,4BD), QJM, 2008, 101, 1, 23-9.
- [20] McDonough M, Kennedy N, Glasper A, Bearn J. Clinical features and management of gamma-hydroxybutyrate (GHB) withdrawal: a review. Drug Alcohol Depend. 2004;75(1):3–9
- [21] Snead OC, III, Gibson KM. Gamma-hydroxybutyric acid. N Engl J Med. 2005;352(26):2721–32.
- [22] Kaupmann K, Cryan JF, Wellendorph P, Mombereau C, Sansig G, Klebs K, Schmutz M, Froestl W, van der Putten H, Mosbacher J, et al. Specific gamma-hydroxybutyrate-binding sites but loss of pharmacological effects of gamma-hydroxybutyrate in GABA(B)(1)-deficient mice. Eur J Neurosci. 2003;18(10):2722–30
- [23] Snead OC, III, Liu CC. GABAA receptor function in the gamma-hydroxybutyrate model of generalized absence seizures. Neuropharmacology. 1993;32(4):401–9
- [24] LeTourneau JL, Hagg DS, Smith SM. Baclofen and gamma-hydroxybutyrate withdrawal. Neurocrit Care. 2008;8:430–433
- [25] Rama M Kamal, Arnt Schellekens, Cornelis AJ De Jong, and Boukje AG Dijkstra. Baclofen as relapse prevention in the treatment of Gamma- Hydroxybutyrate (GHB) dependence: an open label study BMC Psychiatry. 2015; 15: 91.
- [26] Kamal RM, Qurishi R, De Jong CA. Baclofen and ?-hydroxybutyrate (GHB), a dangerous combination. J Addict Med. 2015 Jan-Feb;9(1):75-7













